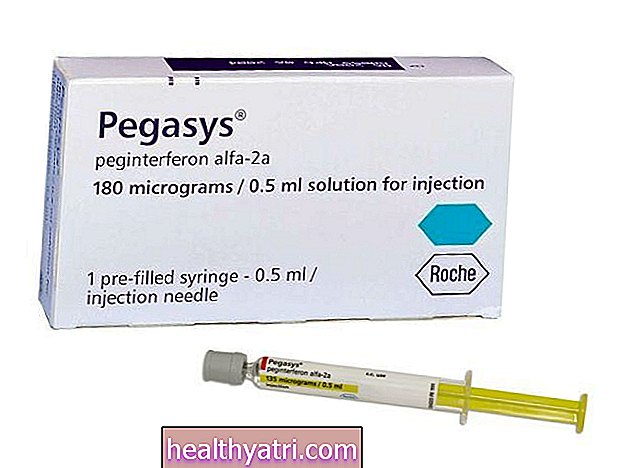
Heplisav-B je vakcína používaná k prevenci všech podtypů hepatitidy B. Byla schválena Úřadem pro kontrolu potravin a léčiv (FDA) USA dne 9. listopadu 2017 pro použití u dospělých ve věku 18 let a starších.
Je to jedna ze tří vakcín, které se v současné době používají k prevenci infekce virem hepatitidy B (HBV) ve Spojených státech. Mezi ně patří Recombivax HB, který byl schválen FDA v roce 1986, a lídr na trhu Engerix-B, kterému bylo podobné schválení uděleno v roce 2007. (Existuje také třetí kombinovaná vakcína známá jako Twinrix, která očkuje proti hepatitidě A i B .)
Jednou z hlavních výhod přípravku Heplisav-B je to, že vyžaduje méně injekcí po kratší dobu, což je faktor, který lidem může pomoci tuto sérii dokončit, místo aby ji zastavili.
Universal Images Group / Universal Images Group / Getty Images
Počáteční obavy o bezpečnost
Schválení Heplisav-B vyvrcholilo čtyřletým bojem o uvedení vakcíny na trh. FDA předtím drogu odmítl v únoru 2013 a později v listopadu 2016 kvůli bezpečnostním obavám ohledně možného rizika akutního infarktu myokardu (infarkt) a některých autoimunitních onemocnění.
Vakcína byla nakonec schválena do značné míry na základě skutečnosti, že vyžaduje dva výstřely podané s odstupem jednoho měsíce. Ostatní vakcíny naopak vyžadují tři injekce oddělené měsícem a poté šesti měsíci.
To bylo považováno za důležité, protože jednou z největších překážek vakcinace proti HBV byla adherence. Studie z roku 2008, kterou provedlo ministerstvo infekčních nemocí na Floridské univerzitě v Jacksonville, uvádí, že ze 707 osob způsobilých k očkování proti HBV pouze 503 přistoupilo k léčbě a pouze 356 absolvovalo sérii tří výstřelů. Jiné studie uvádějí podobně skličující výsledky.
Zmenšením rozdílu mezi injekcemi se FDA domnívá, že výhody vakcíny daleko převažují nad možnými důsledky.
Účinnost
Schválení přípravku Heplisav-B bylo založeno na údajích ze tří klinických studií zahrnujících více než 14 000 dospělých účastníků. Klíčová studie porovnávala dvoudávkovou léčbu přípravkem Heplisav-B se sérií tří dávek přípravku Engerix-B. Mezi 6665 účastníky studie dosáhlo 95% vysoké úrovně ochrany před Heplisav-B (měřeno aktivitou protilátek) ve srovnání s 81% u Engerix-B.
Ve druhé studii zahrnující 961 osob s diabetem typu 2 (považovaných za osoby s vysokým rizikem hepatitidy B) bylo hlášeno, že přípravek Heplisav-B poskytuje vysokou úroveň ochrany u 90% osob, kterým byla vakcína podána, oproti pouze 65% u osob, kterým byl podán přípravek Engerix -B.
Navíc je známo, že Heplisav-B poskytuje ochranu proti všem čtyřem hlavním sérotypům, deseti genotypům (A až J) a 40 subgenotypům.
Správa
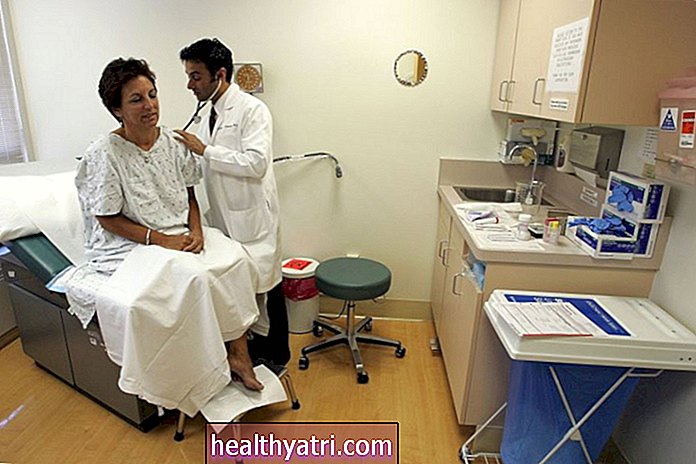
Heplisav-B se dodává intramuskulární injekcí do horního deltového svalu ramene. Vakcína není živá vakcína (obsahující živý oslabený virus), ale obsahuje geneticky modifikovaný antigen - v podstatě avatar viru - který nezpůsobuje onemocnění, ale spíše stimuluje ochrannou imunitní odpověď.
Poté, co vám byla podána první injekce o objemu 0,5 mililitru (ml), bude za šest měsíců dodána druhá.
Pokud z nějakého důvodu nejste schopni dokončit sérii během této doby, poraďte se s lékařem o dokončení série co nejdříve. Je nepravděpodobné, že byste museli sérii restartovat.
Nežádoucí účinky
I když u některých lidí může dojít k reakci na výstřel, většina případů je mírná a vyřeší se během několika dnů. Obecně řečeno, reakce, pokud existují, mají tendenci být hlubší po prvním výstřelu a méně po druhém.
Mezi nejčastější příznaky (vyskytující se u více než 2% pacientů) patří:
- Otok v místě vpichu: 2,3%
- Zarudnutí v místě vpichu: 4,1%
- Malátnost: 9,2%
- Bolest hlavy: 16,9%
- Únava: 17,4%
- Bolest v místě vpichu: 38,5%
Kontraindikace
Přípravek Heplisav-B by neměly užívat osoby s anamnézou závažných alergických reakcí nebo osoby, které již dříve reagovaly na vakcínu proti hepatitidě B nebo na kteroukoli z jejích složek, včetně kvasinek. Opětovné vystavení by mohlo vést k potenciálně život ohrožující alergické reakci celého těla známé jako anafylaxe.
Doposud nebyly provedeny žádné studie u člověka týkající se účinku přípravku Heplisav-B během těhotenství nebo kojení. Studie na zvířatech však nehlásila žádné nežádoucí účinky ani u březích laboratorních potkanů, ani u jejich potomků po dávce 0,3 ml Heplisav-B.
Kdo by měl být očkován
Hepatitida B je virové onemocnění jater, které se může stát chronickým a vést k cirhóze, rakovině jater a smrti.
Podle zprávy pracovní skupiny USA Preventive Services Task Force (USPSTF), kdekoli od 700 000 do 2,2. Předpokládá se, že ve Spojených státech je infikováno HBV milion lidí. Míra infekcí je nejvyšší u dospělých ve věku 30 až 49 let, z nichž většina je nakažena buď nechráněným sexem, nebo sdíleným používáním jehly.
Léčba hepatitidy B neexistuje, ale účinné očkování může této nemoci zabránit. Z tohoto důvodu Poradní výbor pro imunizační postupy (ACIP) a v současné době doporučuje, aby všechny děti dostaly první dávku vakcíny proti HBV při narození a sérii dokončily mezi šesti a 18 měsíci. Měly by být očkovány i starší děti a dospívající, kteří nedostali vakcínu HBV.
Centrum pro kontrolu a prevenci nemocí dále doporučuje očkovat všechny dospělé osoby s vysokým rizikem HBV. Tyto zahrnují:
- Osoby, které žijí nebo mají sex s někým, kdo má hepatitidu B.
- Sexuálně aktivní osoby, které nejsou v dlouhodobém vzájemně monogamním vztahu
- Osoby, které hledají testování nebo léčbu sexuálně přenosné infekce
- Muži, kteří mají sex s muži
- Lidé žijící s HIV
- Lidé, kteří sdílejí jehly, stříkačky nebo jiné příslušenství k drogám
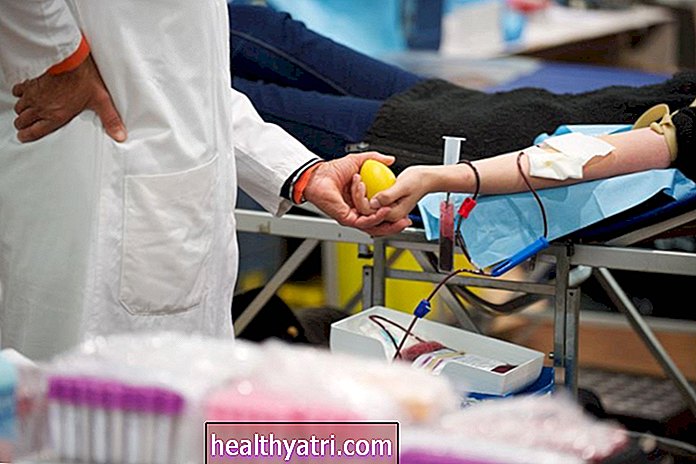
- Zdravotničtí pracovníci a další osoby vystavené riziku vystavení krvi
- Lidé s konečným stadiem onemocnění ledvin
- Lidé s chronickým onemocněním jater
- Lidé s diabetem ve věku do 60 let začali co nejdříve po stanovení diagnózy
- Mezinárodní cestující do regionů se střední až vysokou mírou hepatitidy B.
- Osoby, které se přistěhovaly ze zemí se střední až vysokou mírou hepatitidy B, nebo děti narozené rodičům, kteří se přistěhovali z těchto zemí před jejich narozením
- Každý, kdo se považuje za ohroženého
USPSTF v současné době nedoporučuje očkování proti HBV pro běžnou dospělou populaci, protože se neprokázalo, že by praxe snižovala riziko onemocnění jater nebo úmrtí.
Zkoumání bezpečnostních obav
Navzdory převážně pozitivnímu přijetí ze strany úředníků v oblasti veřejného zdraví obavy o bezpečnost nadále trápí vakcínu vzhledem k jejímu dřívějšímu odmítnutí FDA.
FDA zpočátku odmítla vakcínu v roce 2013 na základě jedné z jejích složek, známé jako CpG 1018. Jedná se o sloučeninu používanou k posílení imunitní spouštěcí schopnosti vakcíny a právě ta, která umožňuje sérii dvou pokusů.
Podle odpovědi FDA se předpokládalo, že CpG 1018 má potenciál vyvolat určité autoimunitní poruchy, včetně onemocnění štítné žlázy. Zatímco rané studie neprokázaly žádný statistický rozdíl mezi Heplisav-B a Engerix-B, přihláška byla zamítnuta jednoduše proto, že velikost studie byla v té době považována za příliš malou.
V době opětovného použití bylo vakcíně vystaveno 14 238 lidí, přičemž byly hlášeny pouze dva případy Hashimotovy tyroiditidy (forma onemocnění štítné žlázy) a jeden případ vitiliga.
Později, v roce 2016, byla vakcína také odmítnuta, když jedna studie uváděla větší než očekávaný počet srdečních příhod, včetně infarktů. V tomto případě FDA požadoval další informace týkající se jakýchkoli neasociovaných faktorů, které by mohly pomoci lépe vysvětlit výsledky.
Po přezkoumání dalších údajů FDA udělil souhlas. Konečné výsledky studie uváděly 0,1% riziko infarktu u lidí, kterým byl podáván přípravek Heplisav-B, oproti 0,2%, kterým byl podáván přípravek Engerix-B.