Verywell / Vincent Iannelli
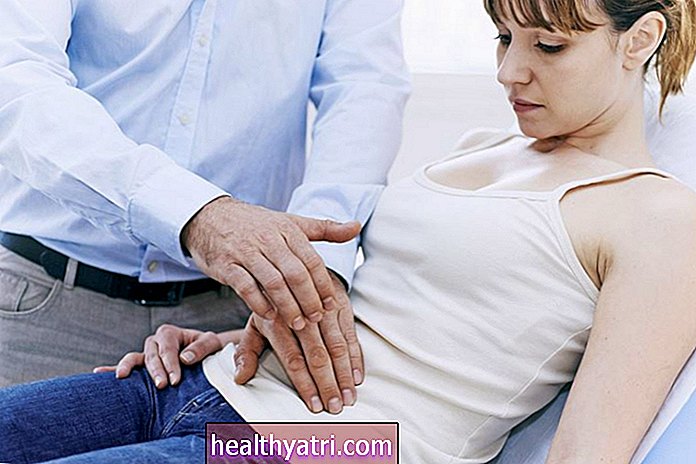
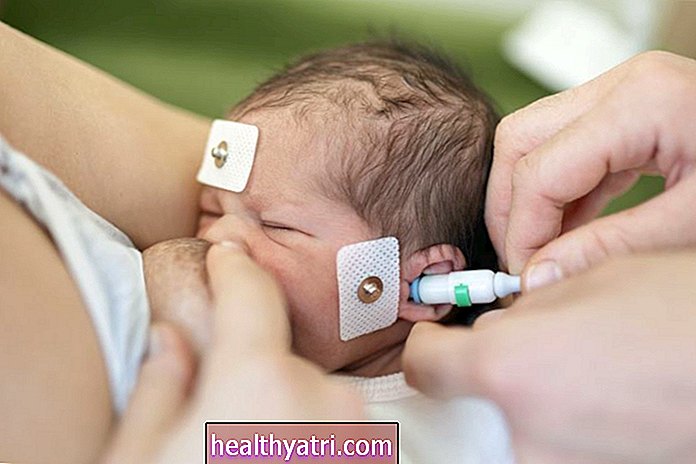
Advair (flutikason + salmeterol) je inhalační lék používaný k léčbě astmatu a chronických obstrukčních plicních onemocnění (CHOPN), včetně emfyzému a / nebo chronické bronchitidy.
V roce 2003 dostal Advair varování před černou skříní od amerického Úřadu pro kontrolu potravin a léčiv (FDA), který radí, že salmeterol může potenciálně zvýšit riziko život ohrožujících astmatických záchvatů. Upozornění na černou skříňku bylo odstraněno v prosinci 2017. Zjistěte proč.
Pochopení varování Black Box
Varování na černou skříňku je preventivní prohlášení vydané FDA, které má informovat veřejnost, že lék může způsobit vážné nebo život ohrožující škody. „Černá skříňka“ doslova odkazuje na odvážně vykreslenou krabičku na informacích o balení, která obsahuje doporučení FDA.
Varování před černou skříní jsou obvykle vydávána kvůli výsledkům klinických studií, které mohou být provedeny poté, co byl lék již schválen a zpřístupněn. Pokud se po schválení léku objeví vážné obavy o bezpečnost, FDA nařídí okamžitou revizi informací o balení. Rovněž budou rozptýlena média, aby varovala veřejnost před obavami.
Obavy FDA o Advair
V roce 2003 klinická studie s názvem Salmeterol Multicenter Asthma Research Trial (SMART) zjistila, že salmeterol byl spojen s malým, ale významným zvýšením rizika úmrtí a hospitalizace u lidí s astmatem, zejména afrických Američanů. Na základě těchto zjištění bylo vydáno varování o černé krabičce týkající se všech a všech léků obsahujících salmeterol, včetně Advairu.
Studie dále uvádí podobné riziko úmrtí a hospitalizace s formoterolem, lékem patřícím do stejné třídy léků známých jako dlouhodobě působící beta agonisté (LABA).
Pokud jsou použity samostatně, LABA neposkytují dostatečnou úlevu od příznaků. Kromě toho mohou LABA, pokud se používají samostatně, vyvolat astmatické záchvaty.
Z tohoto důvodu byly poprvé vytvořeny společně formulované léky, jako je Advair, který také obsahuje inhalační kortikosteroid (ICS).
Při použití s ICS lze nepříznivé účinky LABA do značné míry zmírnit.
Když byla studie později přezkoumána, vyšlo najevo, že jedinci, kteří užívali LABA s ICS, neměli větší nebo menší riziko úmrtí nebo hospitalizace než ti, kteří užívali samotný kortikosteroid. Většina vědců dnes uznává, že studie SMART byla špatně navržena a vyloučila faktory, které by jinak mohly anomálii vysvětlit.
Co dnes říká FDA
V roce 2016 byly vydány první v novém kole studií Advair pověřených FDA.
Studie AUSTRI hodnotila bezpečnost samotného flutikasonu vs. kombinace salmeterolu a flutikasonu u 11 679 lidí s astmatem, z nichž někteří byli již ve věku 12. Vyšetřovatelé zajistili, že 15% účastníků byli Američané z Afriky, aby mohli lépe určit, zda mohou být nežádoucí účinky související s rasou.
Vyšetřovatelé zjistili, že riziko astmatických záchvatů nebo jiných nežádoucích účinků nebylo u účastníků užívajících salmeterol-flutikason vyšší než u těch, kteří užívali samotný flutikason (kortikosteroid).
Studie potvrdila, že Advair dodáváním LABA a kortikosteroidů v jediném produktu nepředstavuje žádné z rizik navrhovaných ve varování FDA před černou krabičkou.
Zatímco FDA zachovává varování černé skříňky u produktů, které používají samotné LABA, léky obsahující ICS i LABA obsahujíVarování a opatřenípřipomínat uživatelům rizika používání LABAbezICS. Léky, které obsahují ICS i LABA, jsou schváleny FDA pro léčbu astmatu a CHOPN.