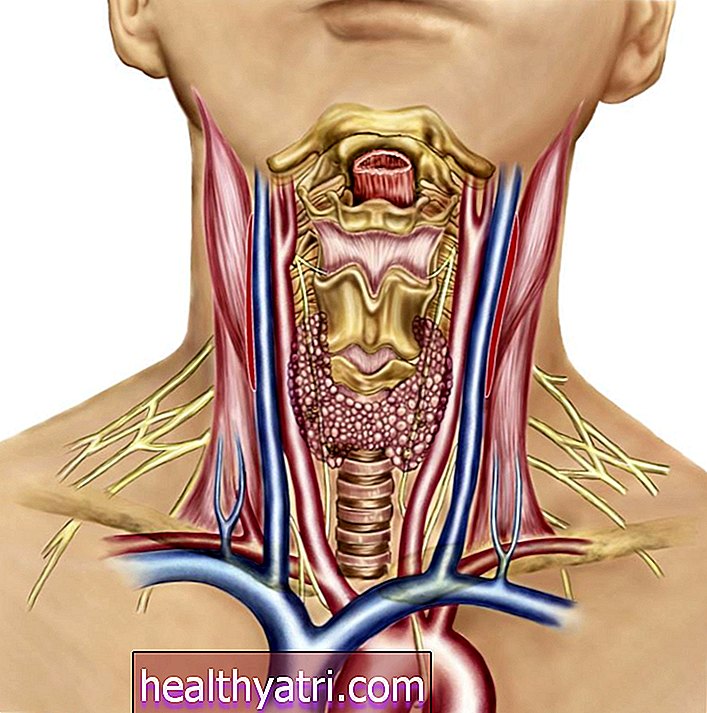
Schopnost lidského těla regenerovat tkáně a orgány je extrémně neúčinná a ke ztrátě lidské tkáně a orgánů může dojít snadno kvůli věcem, jako jsou vrozené vady, nemoci a náhlé trauma. Když tkáň zemře (nazývá se nekróza), nelze ji přivést zpět k životu - pokud nebude odstraněna nebo opravena, může to mít vliv na jiné oblasti těla, jako je okolní tkáň, orgány, kosti a kůže.
To je místo, kde je užitečné tkáňové inženýrství. Pomocí biomateriálu (hmoty, která interaguje s biologickými systémy těla, jako jsou buňky a aktivní molekuly), lze vytvořit funkční tkáně, které pomáhají obnovit, opravit nebo nahradit poškozenou lidskou tkáň a orgány.
Cavan Images / Getty ImagesStručná historie
Tkáňové inženýrství je relativně nová oblast medicíny a výzkum začíná teprve v 80. letech. Americký bioinženýr a vědec jménem Yuan-Cheng Fung předložil Národní vědecké nadaci (NSF) návrh, aby bylo výzkumné centrum věnováno živým tkáním. Fung přijal koncept lidské tkáně a rozšířil jej tak, aby platil pro jakýkoli živý organismus mezi buňkami a orgány.
Na základě tohoto návrhu označil NSF termín „tkáňové inženýrství“ ve snaze vytvořit novou oblast vědeckého výzkumu. To vedlo k založení The Tissue Engineering Society (TES), která se později stala Tissue Engineering and Regenerative Medicine International Society (TERMIS).
TERMIS podporuje vzdělávání i výzkum v oblasti tkáňového inženýrství a regenerativní medicíny. Regenerativní medicína se týká širší oblasti, která se zaměřuje jak na tkáňové inženýrství, tak na schopnost lidského těla se samoléčit, aby obnovila normální funkci tkáně, orgánů a lidských buněk.
Účel tkáňového inženýrství
Tkáňové inženýrství má v medicíně a výzkumu několik hlavních funkcí: pomoc s opravou tkání nebo orgánů, včetně opravy kostí (kalcifikovaná tkáň), tkáně chrupavky, srdeční tkáně, tkáně pankreatu a vaskulární tkáně. Pole také provádí výzkum chování kmenových buněk. Kmenové buňky se mohou vyvinout do mnoha různých typů buněk a mohou pomoci opravit oblasti těla.
Oblast tkáňového inženýrství umožňuje vědcům vytvářet modely pro studium různých nemocí, jako je rakovina a srdeční choroby.
3D povaha tkáňového inženýrství umožňuje studovat architekturu nádorů v přesnějším prostředí. Tkáňové inženýrství také poskytuje prostředí pro testování potenciálních nových léků na tato onemocnění.
Jak to funguje
Proces tkáňového inženýrství je komplikovaný. Zahrnuje vytvoření 3D funkční tkáně, která pomáhá opravit, nahradit a regenerovat tkáň nebo orgán v těle. K tomu jsou buňky a biomolekuly kombinovány s lešeními.
Lešení jsou umělé nebo přírodní struktury, které napodobují skutečné orgány (například ledviny nebo játra). Tkáň roste na těchto lešeních, aby napodobovala biologický proces nebo strukturu, kterou je třeba vyměnit. Když jsou tyto konstruovány společně, je vytvořena nová tkáň, která replikuje stav staré tkáně, když nebyla poškozena nebo nemocná.
Lešení, buňky a biomolekuly
Lešení, která jsou normálně vytvářena buňkami v těle, lze postavit ze zdrojů, jako jsou bílkoviny v těle, umělé plasty, nebo ze stávajícího lešení, například z dárcovského orgánu. V případě dárcovského orgánu by bylo lešení kombinováno s buňkami pacienta, aby se vytvořily přizpůsobitelné orgány nebo tkáně, které by imunitní systém pacienta pravděpodobně odmítl.
Bez ohledu na to, jak je vytvořen, je to tato struktura lešení, která odesílá zprávy do buněk, které pomáhají podporovat a optimalizovat funkce buněk v těle.
Výběr správných buněk je důležitou součástí tkáňového inženýrství. Existují dva hlavní typy kmenových buněk.
Dva hlavní typy kmenových buněk
- Embryonální kmenové buňky: pocházejí z embryí, obvykle ve vejcích, která byla oplodněna in vitro (mimo tělo).
- Kmenové buňky pro dospělé: nacházejí se v těle mezi běžnými buňkami - mohou se množit buněčným dělením a doplňovat tak umírající buňky a tkáně.
V současné době probíhá spousta výzkumů i na pluripotentních kmenových buňkách (dospělých kmenových buňkách, u kterých se indukuje, že se chovají jako embryonální kmenové buňky). Teoreticky existuje neomezený přísun pluripotentních kmenových buněk a jejich použití nezahrnuje problém ničení lidských embryí (což také způsobuje etický problém). Výzkumníci, kteří získali Nobelovu cenu, zveřejnili svá zjištění týkající se pluripotentních kmenových buněk a jejich použití.
Celkově biomolekuly zahrnují čtyři hlavní třídy (i když existují i sekundární třídy): sacharidy, lipidy, proteiny a nukleové kyseliny. Tyto biomolekuly pomáhají tvořit buněčnou strukturu a funkci. Sacharidy pomáhají orgánům, jako je mozek a srdce, stejně jako systémy fungují jako zažívací a imunitní systém.
Proteiny poskytují protilátky proti choroboplodným zárodkům, stejně jako strukturální podporu a pohyb těla. Nukleové kyseliny obsahují DNA a RNA a dávají buňkám genetickou informaci.
Lékařské použití
Tkáňové inženýrství se v péči nebo léčbě pacientů příliš nepoužívá. Vyskytlo se několik případů, kdy se u pacientů použilo tkáňové inženýrství při kožních štěpech, opravách chrupavek, malých tepnách a močových měchýřích. Větší orgány tkáňového inženýrství, jako je srdce, plíce a játra, však u pacientů dosud nebyly použity (i když byly vytvořeny v laboratořích).
Kromě rizikového faktoru použití tkáňového inženýrství u pacientů jsou postupy extrémně nákladné. Tkáňové inženýrství je užitečné, pokud jde o lékařský výzkum, zejména při testování nových lékových formulací.
Používání živé, fungující tkáně v prostředí mimo tělo pomáhá vědcům získat zisky v personalizované medicíně.
Personalizovaná medicína pomáhá určit, zda některé léky fungují lépe pro určité pacienty na základě jejich genetického složení, a také snižuje náklady na vývoj a testování na zvířatech.
Příklady tkáňového inženýrství
Nedávný příklad tkáňového inženýrství prováděného Národním ústavem pro biomedicínské zobrazování a bioinženýrství zahrnuje inženýrství lidské jaterní tkáně, která je poté implantována do myši. Protože myš používá vlastní játra, lidská jaterní tkáň metabolizuje léky, což napodobuje, jak by lidé reagovali na určité léky uvnitř myši. To pomáhá vědcům zjistit, jaké jsou možné lékové interakce s určitými léky.
Ve snaze o vytvoření tkáně s vestavěnou sítí vědci testují tiskárnu, která by vytvořila vaskulární síť z roztoku cukru. Roztok by se vytvořil a ztvrdl ve vytvořené tkáni, dokud nebude do procesu přidána krev, která cestuje uměle vytvořenými kanály.
A konečně, regenerace ledvin pacienta pomocí vlastních buněk pacienta je dalším projektem ústavu. Vědci použili buňky z dárcovských orgánů ke spojení s biomolekulami a kolagenovým lešením (z dárcovského orgánu) k pěstování nové tkáně ledvin.
Tato orgánová tkáň byla poté testována na fungování (například absorpci živin a produkci moči) jak venku, tak i uvnitř krys. Pokrok v této oblasti tkáňového inženýrství (který může obdobně fungovat i pro orgány, jako je srdce, játra a plíce) by mohl pomoci s nedostatkem dárců a snížit jakákoli onemocnění spojená s imunosupresí u pacientů po transplantaci orgánů.
Jak to souvisí s rakovinou
Metastatický růst nádoru je jedním z důvodů, proč je rakovina hlavní příčinou úmrtí. Před tkáňovým inženýrstvím bylo možné vytvořit prostředí nádoru pouze mimo tělo ve 2D formě. Nyní 3D prostředí, stejně jako vývoj a využití určitých biomateriálů (jako je kolagen), umožňují vědcům podívat se na prostředí nádoru až do mikroprostředí určitých buněk, aby zjistili, co se stane s nemocí, když se změní určité chemické složení v buňkách .
Tímto způsobem tkáňové inženýrství pomáhá vědcům pochopit jak progresi rakoviny, tak i to, jaké účinky mohou mít určité terapeutické přístupy na pacienty se stejným typem rakoviny.
Zatímco bylo dosaženo pokroku ve studiu rakoviny prostřednictvím tkáňového inženýrství, růst nádoru může často způsobit tvorbu nových krevních cév. To znamená, že i přes pokrok, který tkáňové inženýrství dosáhlo při výzkumu rakoviny, mohou existovat omezení, která lze eliminovat pouze implantací upravené tkáně do živého organismu.
U rakoviny však může tkáňové inženýrství pomoci zjistit, jak se tyto nádory formují, jak by měly vypadat normální buněčné interakce a jak rakovinné buňky rostou a metastazují. To pomáhá vědcům testovat léky, které ovlivní pouze rakovinné buňky, na rozdíl od celého orgánu nebo těla.












-and-people-with-dementia.jpg)