Ektopická označuje předmět nebo lidskou tkáň, která se tvoří nebo se nachází tam, kam nepatří. Ektopická tvorba kostí je ukládání nového kostního materiálu (procesem zvaným osifikace) v oblastech, kam tento materiál opět nepatří. Tento proces osifikace se provádí buňkami zvanými osteoblasty.
Cecilie_Arcurs / Getty ImagesSlovo ektopické pochází od Řeků a znamená „daleko od místa“. Jeho antonymum, které je „ortotopickou“ kostí - odvozenou také z řečtiny - označuje kosti, které jsou vytvořeny ve správném anatomickém umístění, tvrdí Scott, et. al., ve svém článku nazvaném „Stručný přehled modelů formování ektopické kosti“. Článek byl publikován v časopise z března 2012,Vývoj kmenových buněk.
Ektopická tvorba kostí může být přítomna při narození, může být způsobena genetikou nebo může vzniknout jako komplikace určitých zdravotních stavů, jako je paraplegie a / nebo traumatické poranění (abychom jmenovali jen několik). Scott, et. al. říkají, že se předpokládá, že tvorba ektopické kosti je způsobena lokálním zánětem, po kterém následuje shromáždění kosterních progenitorových buněk. Podle webu Bostonské dětské nemocnice je progenitorová buňka hodně podobná kmenové buňce, až na to, že je omezenější, pokud jde o typy buněk, které se mohou stát při dělení. Progenitorové buňky pocházejí z kmenových buněk, ale nejsou to dospělé kmenové buňky.
Ektopická kostní formace v důsledku operace páteře
Scott, et. al, říkají, že až u 10% pacientů, kteří podstoupí invazivní chirurgii - a operace zad určitě spadá do této skupiny - se vyvine ektopická tvorba kostí.
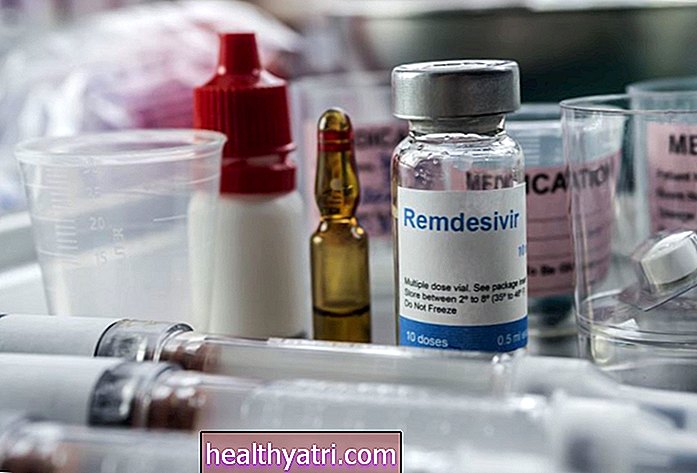
V páteři se termín „ektopická tvorba kostí“ někdy používá k popisu nežádoucí kostní tkáně, která se ukládá v míšním kanálu. V roce 2002 schválila FDA kostní protein vyrobený společností Medtronic s názvem Infuse pro použití při operacích bederní páteře. Kritéria použití specifikovaná FDA byla velmi specifická: Jako kostní štěp pro jednoúrovňový Anterior Lumbar Interbody Fusion (ALIF) v systému Lumbar Tapered Fusion Device (LT-Cage).
Ale brzy po schválení začalo mnoho chirurgů používat materiál „mimo značku“, což znamená pro jiné účely, než jaké schválil FDA. Nesprávné použití zahrnovalo operaci krční páteře, která vedla k řadě „nežádoucích účinků“ nebo k hlášení AE FDA. Ektopická tvorba kostí byla jedním z AE, ale seznam zahrnoval další velmi závažné věci, jako je arachnoiditida, zvýšené neurologické deficity, retrográdní ejakulace, rakovina a další. Není to hezké.
Kontroverze Medtronic
TheMilwaukee Journal SentinalHlídací pes, který tento příběh sleduje od roku 2011 (a pokračuje v něm), uvádí, že během několika týdnů od prvního klinického hodnocení přípravku Infuse byla u 70% pacientů studie zjištěna ektopická tvorba kostí. Někteří z těchto pacientů vyžadovali jeden nebo více chirurgických zákroků k nápravě nežádoucí kosti a / nebo zdravotních komplikací, které z ní vznikly.
Ve svém přezkumu důkazů zveřejněných v čísle z roku 2013Surgery Neurology International, Epstein porovnal 13 průmyslových studií s jinými studiemi následně publikovanými v časopisech, stejně jako s dokumenty a informacemi FDA umístěnými v databázích. Uvádí, že ve studiích Infuse zjistila „původně nepublikované nepříznivé události a vnitřní nekonzistence“. Rovněž uvádí, že 40% nežádoucích účinků lze přičíst ALIF („off-label“ operace krku, která byla provedena,) a dodává, že některé z těchto příhod byly život ohrožující.
MezitímMilwaukee Journal Sentineluvádí, že společnost Medtronic ve zprávě z roku 2004, kterou napsali lékaři financovaní společností Medtronic, hlásila tyto nežádoucí účinky FDA buď nedostatečně, nebo vůbec. MJS říká, že „lékaři, kteří napsali dokument z roku 2004, budou nadále dostávat miliony dolarů na licenčních poplatcích a dalších platbách od společnosti Medtronic.“
V květnu 2014 MJS navázala na tento příběh dalším článkem, v němž se uvádí, že společnost Medtronic souhlasila se zaplacením 22 milionů dolarů na vypořádání 1000 pohledávek proti jejich společnosti Infuse. Příběh také zmínil, že společnost Medtronic vyčleňuje dalších 140 milionů dolarů na pokrytí „očekávaných nároků“.









-for-rescuer-safety.jpg)