Sasiistock / Getty Images
Klíčové jídlo
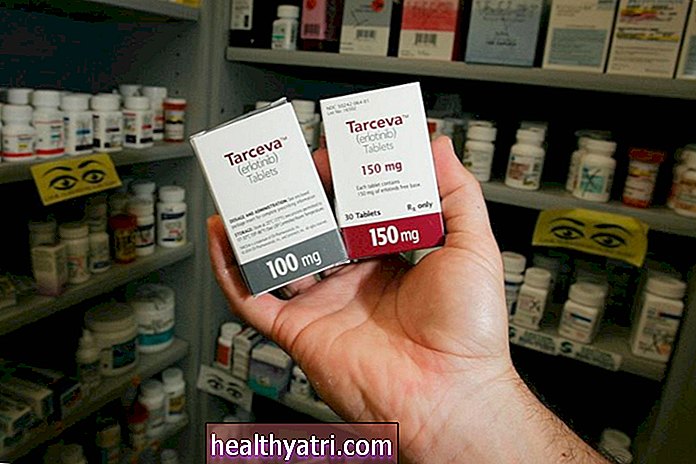
- Společnost Pfizer získala souhlas FDA k zahájení testování své vakcíny proti koronavirům u dětí ve věku 12 let a starších.
- Odborníci tvrdí, že zahrnutí dětí do klinických studií je zásadní pro celkový vývoj vakcíny, která bude chránit děti i dospělé před COVID-19.
- Podle svých webových stránek společnost Pfizer do své studie již zapojila více než 39 000 dobrovolníků. Více než 34 000 těchto dobrovolníků již podstoupilo druhé očkování.
Americká farmaceutická společnost Pfizer v říjnu oznámila, že obdržela povolení od amerického Úřadu pro kontrolu potravin a léčiv (FDA) k zahájení zápisu dětí ve věku do 12 let do studií s vakcínami proti koronavirům.
"Tímto způsobem budeme schopni lépe porozumět potenciální bezpečnosti a účinnosti vakcíny u jedinců více věkových skupin a původů," uvedla společnost v aktualizovaném prohlášení.
Půjde o první studii vakcíny COVID-19 v USA, do které budou zařazeny děti. Od října je společnost Pfizer jednou ze čtyř amerických společností, které mají vakcíny v klinických studiích fáze 3.
Společnost Pfizer již rozšířila fázi 3 své studie o děti ve věku 16 let a starší, jakož i osoby s chronickým stabilním virem lidské imunodeficience (HIV), hepatitidou C a hepatitidou B.
Proč testovat vakcínu COVID-19 u dětí?
Než společnost Pfizer získala souhlas k zahájení testování u dětí, odborníci zveřejnili zprávu v časopiseKlinické infekční nemocis uvedením důležitosti takového testování.
„Přímý dopad COVID-19 na děti je větší, než jaký byl pozorován u řady dalších patogenů, pro které nyní máme účinné pediatrické vakcíny,“ uvádí se ve zprávě. "Navíc role dětí v přenosu SARS-CoV-2 byla zjevně nedoceněná." Pečlivě provedené klinické studie fáze 2 mohou adekvátně vyřešit potenciální obavy o bezpečnost vakcín COVID-19. “
MUDr. Suzanne Pham
Šíření tohoto viru nemůžeme překonat, dokud neočkujeme své děti.
- MUDr. Suzanne PhamSharon Nachman, MD, vedoucí oddělení dětských infekčních nemocí v dětské nemocnici Stony Brook v New Yorku, souhlasí se zprávou a říká Verywell, že „pediatři mají velký zájem vidět podrobnosti studie a jak bude vakcína fungovat u dětí . “
Testování vakcíny u dětí má podle Nachmana specifické výhody. Vědci budou schopni posoudit krátkodobou a dlouhodobou imunitní odpověď, která zahrnuje zjištění, zda je dávka vakcíny použitá u dospělých pro děti nezbytná, nebo zda by měla podobnou imunitní odpověď jako nižší dávka.
Nachman říká, že je také důležité si uvědomit, že protože koronavirům u dospělých může předcházet jejich expozice asymptomatické infekci u dětí, mohlo by zavedení vakcíny k léčbě celé rodiny „vést dlouhou cestu k omezení přenosu doma i v komunitě“.
MUDr. Suzanne Pham, vedoucí lékařka v nemocnici Weiss Memorial Hospital v Chicagu, říká Verywell, že čím dříve mohou být děti očkovány, tím dříve se sníží přenosová rychlost.
„Účinným očkováním dětí se sníží riziko přenosu viru v komunitě, zejména u vysoce rizikových lidí, kteří jsou náchylnější k závažným nebo kritickým onemocněním,“ říká Pham Verywell. "To umožní, aby školy začaly znovuotevírat a kontrolovaně obnovovat činnosti zásadní pro rozvoj našich dětí." Šíření tohoto viru nemůžeme překonat, dokud neočkujeme své děti. Musíme mít ve společnosti dostatek stádové imunity, abychom byli schopni zabránit šíření. “
Vakcíny COVID-19: Mějte přehled o tom, jaké vakcíny jsou k dispozici, kdo je může získat a jak bezpečné jsou.
Jak začínají vakcíny?
Pham vysvětluje, že pro testování vakcíny - na dospělých nebo dětech - musí společnost nejprve předložit FDA žádost Investigational New Drug (IND).
Aplikace bude popisovat vakcínu, jak je vyráběna a jaké testy kontroly kvality mají být použity. Aplikace také obsahuje údaje ze zkoušek na zvířatech, které prokazují, že vakcína je pro počáteční testování u lidí bezpečná.
Jak vysvětluje FDA, proces aplikace má několik kroků:
Během raného předklinického vývoje nového léku je hlavním cílem sponzora určit, zda je produkt přiměřeně bezpečný pro počáteční použití u lidí a zda sloučenina vykazuje farmakologickou aktivitu, která ospravedlňuje komerční vývoj.
Pokud je produkt identifikován jako životaschopný kandidát pro další vývoj, zadavatel se poté soustředí na shromažďování údajů a informací nezbytných k prokázání, že produkt nebude při omezených počátečních klinických studiích vystavovat člověka nepřiměřeným rizikům.
Vakcína poté projde zkouškami fáze 1, což Pham vysvětluje jako „studie bezpečnosti a imunogenity prováděné u malého počtu lidských subjektů, které jsou pečlivě sledovány.“
„Fáze 2 sestává ze studií zaměřených na dávku a je rozšířena na větší počet (stovky) lidských subjektů,“ říká Pham. "Poté se pokusy fáze 3 pokusí zaregistrovat tisíce lidských subjektů, aby dokumentovaly účinnost a pokračovaly ve zkoumání bezpečnostních údajů."
Podle svého webu Pfizer do své studie zapsal více než 39 000 dobrovolníků. Více než 34 000 z nich dostalo druhou dávku vakcíny.
Co to pro vás znamená
Klinická studie fáze 3, která zahrnuje testování vakcíny COVID-19 u dětí, je známkou pokroku. S vakcínou však nelze spěchat. Konečné výsledky vyžadují určitou dobu, aby byla zajištěna bezpečnost účastníků studie i dospělých a dětí, které nakonec obdrží hotovou verzi vakcíny.










-subtypes.jpg)