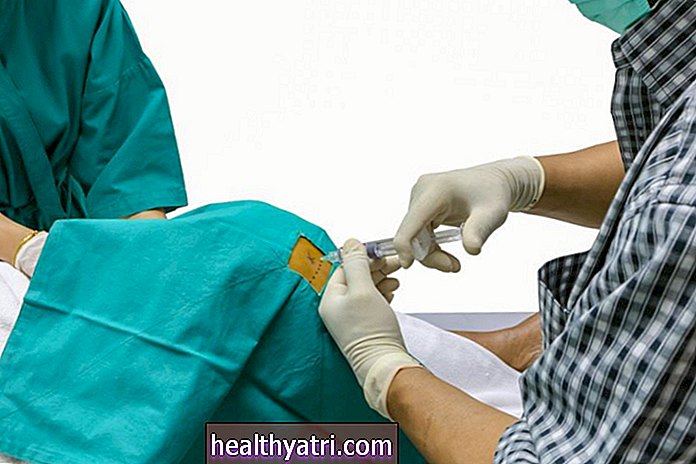
Rasuvo (methotrexát), jednodávkový autoinjektor obsahující lék na předpis methotrexát, bylo schváleno americkým Úřadem pro kontrolu potravin a léčiv (FDA) 11. července 2014. Rasuvo, vyráběné společností Medac, Pharma, Inc., je snadno dostupné použijte alternativu k perorálnímu methotrexátu nebo injekční formě injekční lahvičky a stříkačky.
BURGER / PHANIE / Getty ImagesIndikace
Přípravek Rasuvo je schválen pro léčbu pacientů s těžkou aktivní revmatoidní artritidou a polyartikulární juvenilní idiopatickou artritidou, kteří nedostatečně reagovali na léčbu první volby nebo netolerovali. Přípravek Rasuvo je také indikován ke kontrole příznaků spojených s těžkou, vzpurnou a invalidizující psoriázou u dospělých, u nichž se nepodařilo dosáhnout uspokojivé odpovědi u jiných možností léčby. (Poznámka: Rasuvo by se nemělo používat k léčbě neoplastických onemocnění.)
Správa
Rasuvo se podává jednou týdně pouze jako subkutánní injekce. Rasuvo je k dispozici v 10 dávkách od 7,5 mg do 30 mg (v krocích po 2,5 mg). Autoinjektor se spouští ručně a měl by být injikován do břicha nebo stehna. Pokud je předepsána dávka nižší než 7,5 mg nebo vyšší než 30 mg, nebo pokud je nutná úprava pod 2,5 mg, měly by být použity jiné formulace methotrexátu.
Typická počáteční dávka methotrexátu pro revmatoidní artritidu je 7,5 mg jednou týdně pro orální nebo subkutánní injekci. U psoriázy je obvyklá počáteční dávka 10–25 mg jednou týdně orálně, intramuskulárně, subkutánně nebo intravenózně. U polyartikulární juvenilní idiopatické artritidy je počáteční dávka 10 mg / m2 jednou týdně (m2 je čtvereční metr plochy povrchu těla).
Kdo by neměl používat Rasuvo
Těhotné pacientky s revmatoidní artritidou by neměly přípravek Rasuvo užívat. Měli by se mu také vyhnout kojící matky a pacienti, kteří se zabývají: alkoholismem nebo onemocněním jater, syndromy imunodeficience nebo již existujícími krevními dyskraziemi. Pacienti se známou přecitlivělostí na methotrexát by se měli také Rasuvo vyhnout.
Časté nežádoucí reakce
S přípravkem Rasuvo se vyskytují časté nežádoucí účinky, jako je nevolnost, bolest břicha, dyspepsie, vředy v žaludku nebo v ústech, nasofaryngitida, průjem, abnormality jaterních testů, zvracení, bolest hlavy, bronchitida, trombocytopenie (nízké krevní destičky), alopecie, leukopenie (nízký počet bílých krvinek pancytopenie (nízký počet pro všechny typy krvinek), závratě a citlivost na ultrafialové světlo. Pokud zaznamenáte nežádoucí reakci, můžete ji nahlásit výrobci léků na čísle 1-855-336-3322, FDA na čísle 1-800-FDA-1088 nebo Medwatch.
Lékové interakce
Lékař by měl mít seznam všech léků a doplňků, které v současné době užíváte. Uvědomte si, že užíváním aspirinu, NSAID nebo kortikosteroidů spolu s přípravkem Rasuvo mohou být hladiny methotrexátu v séru prodlouženy (tj. Mohou zůstat v krvi déle) a potenciálně zvyšovat riziko toxicity.
Užívání inhibitorů protonové pumpy (např. Nexium nebo omeprazol) spolu s přípravkem Rasuvo může také prodloužit hladinu methotrexátu v séru a zvýšit riziko toxicity.
Varování a bezpečnostní opatření
Rasuvo obsahuje varování v rámečku (nejzávažnější typ vydaného varování). Parafrázované zvýraznění upozornění v rámečku jsou:
- Přípravek Rasuvo by měli používat pouze lékaři, kteří mají znalosti a zkušenosti s antimetabolitovou terapií. Rasuvo je metabolický inhibitor folátového analogu.
- Vzhledem k možnému výskytu závažných toxických reakcí, které mohou být smrtelné, by měl být přípravek Rasuvo předepisován pouze osobám s revmatoidní artritidou, psoriázou nebo polyartikulární juvenilní idiopatickou artritidou, které nereagovaly na jinou léčbu.
- Methotrexát údajně způsoboval smrt plodu nebo vrozené abnormality.
- Eliminace methotrexátu je snížena u pacientů se zhoršenou funkcí ledvin, ascitem nebo pleurálním výpotkem.
- Útlum kostní dřeně, aplastická anémie a gastrointestinální toxicita se mohou objevit neočekávaně a mohou být potenciálně smrtelné, pokud je methotrexát užíván s NSAID.
- Dlouhodobé užívání methotrexátu může způsobit hepatotoxicitu, fibrózu a cirhózu. Mohou být indikovány pravidelné jaterní biopsie.
- Může se objevit plicní onemocnění vyvolané methotrexátem (např. Akutní a chronická intersticiální pneumonitida), a to i při nižších dávkách.
- Průjem a ulcerózní stomatitida vyžadují ukončení léčby methotrexátem, aby se zabránilo perforaci střev nebo hemoragické enteritidě.
- Maligní lymfom se může vyvinout i při nízké dávce methotrexátu. Lék by měl být vysazen, aby se zjistilo, zda lymfom ustupuje.
- Methotrexát může vyvolat „syndrom rozpadu nádoru“ u pacientů, kteří mají rychle rostoucí nádory.
- Při užívání methotrexátu se mohou objevit závažné, někdy smrtelné kožní reakce.
- Při užívání methotrexátu se mohou objevit potenciálně fatální oportunní infekce.
- Pokud se metotrexát podává společně s radioterapií, může existovat zvýšené riziko nekrózy měkkých tkání a osteonekrózy.
Sečteno a podtrženo
Rasuvo je vhodná formulace methotrexátu. Rasuvo nese všechny potenciální nežádoucí účinky a krabicová varování spojená s jinými formulacemi methotrexátu.

.jpg)