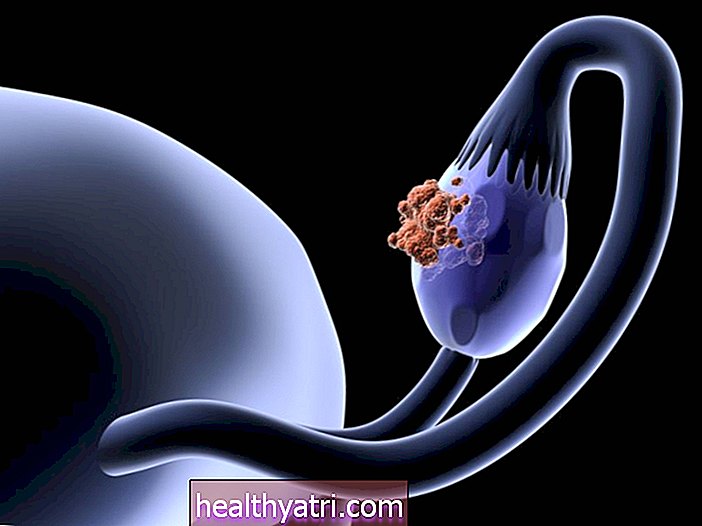
Melflufen (melfalan flufenamid) je nový lék zkoumaný v léčbě relabujícího nebo refrakterního mnohočetného myelomu (RRMM). Je to derivát chemoterapeutického léku melfalan. Melflufen je konjugát peptid-lék; kombinace melfalanu a peptidu (malého proteinu) spojeného dohromady. Melflufen se podává intravenózní infuzí (do žíly).
Lék byl v červenci 2020 předložen americkému Úřadu pro kontrolu potravin a léčiv (FDA) jako nová aplikace. FDA udělil prioritu žádosti a rozhodnutí se očekává na konci února 2021. Melflufen dosud není široce dostupné, protože nebylo licencováno a schváleno pro použití u myelomu. Pacienti však mohou být léčeni tímto přípravkem jako součást klinického hodnocení.
SimpleImages / Getty Images
Co je mnohočetný myelom?
Mnohočetný myelom je typ vzácné, nevyléčitelné rakoviny krve, známé také jako hematologická rakovina. Ovlivňuje buňky zvané plazmatické buňky, což jsou typy bílých krvinek. Léčba mnohočetného myelomu neexistuje a téměř vždy se vrací, kdy se říká, že máte „relabující nebo refrakterní“ onemocnění.
Jak funguje Melflufen?
Jelikož jsou v dřívějších liniích léčby zavedeny nové kombinace anti-myelomových léků, lidé s RRMM často trpí onemocněním, které je rezistentní vůči více lékům, proto jsou naléhavě nutné léky s novými mechanismy účinku.
Melflufen v kombinaci se steroidem dexamethasonem má potenciál naplnit tuto nesplněnou lékařskou potřebu poskytnutím:
- Nový mechanismus působení
- Klinicky významná účinnost
- Spravovatelná bezpečnost
Melflufen ničí myelomové buňky pomocí peptidáz (enzymů, které štěpí peptidy), které se často nacházejí ve vyšším počtu v myelomových buňkách než ve zdravých buňkách. Když melflufen vstupuje do myelomových buněk, peptidázy v buňce rozbijí vazbu držící melfalan a peptidáza dohromady. Tím se v buňce myelomu uvolňuje aktivní melfalan. Melfalan poté způsobí nevratné poškození DNA, což vede k buněčné smrti.
Co říká výzkum
Probíhá výzkum s cílem nalézt nové způsoby léčby mnohočetného myelomu a vypracovat způsoby, jak zlepšit využití stávajících.
Abychom vám pomohli s výzkumem, můžete být během léčby požádáni, abyste se zúčastnili klinického hodnocení.
Melflufen je v současné době zkoumán jako léčba pacientů s RRMM v podmínkách klinických studií. Klinické studie, které zkoumaly účinnost melflufenu, zahrnují:
Studie O-12-M1
O-12-M1 byla mezinárodní multicentrická studie fáze I / II, jejímž cílem bylo stanovit dávku melflufenu v kombinaci s dexamethasonem a zkoumat léčebnou odpověď u pacientů s RRMM, kteří byli refrakterní (rezistentní) vůči poslední linii léčby. Zloženie: 100% bavlna.
Do studie O-12-M1 byla zahrnuta skupina 45 pacientů, kteří podstoupili alespoň dvě předchozí terapie v období od července 2013 do prosince 2016. Cílem studie bylo zjistit maximální tolerovanou dávku melflufenu. Stanovená maximální tolerovaná dávka byla 40 mg melflufenu v kombinaci s dexamethasonem.
Testovaná skupina s nejvyšší dávkou (55 mg) překročila maximální tolerovanou dávku, protože čtyři ze šesti pacientů zaznamenali závažné nežádoucí účinky včetně neutropenie (nízký počet bílých krvinek) a trombocytopenie (nízký počet krevních destiček); plánovaná nejvyšší dávka 70 mg proto nebyla testována.
U pacientů ve studii vedla léčba melflufenem a dexamethasonem ke stabilizaci onemocnění u 76% pacientů.
Medián doby do další léčby - zahájení léčby do další léčby (nebo do smrti pacienta, podle toho, co nastane dříve) - byl 7,9 měsíce. Pacienti žili s mediánem 20,7 měsíce.
Klinická studie HORIZON
V klinické studii fáze II HORIZON - která proběhla na 20 místech po celých Spojených státech a Evropě - byl melflufen a dexamethason podán celkem 154 pacientům, kteří dostali průměrně pět předchozích léčebných linií.
Všichni pacienti byli dříve léčeni imunomodulačním léčivem a inhibitorem proteazomu a byli rezistentní na pomalidomid a / nebo daratumumab.
Asi tři z každých 10 pacientů (29%) odpověděli na léčbu a průměrná doba před návratem myelomu byla čtyři měsíce. Tyto výsledky ukázaly, že melflufen může být přínosný pro pacienty, kteří již dříve podstoupili více linií léčby.
Nežádoucí účinky (AE) vedly ke snížení dávky melflufenu u 27% pacientů a ke zpoždění dávky u 61% pacientů. Nejběžnějším nežádoucím účinkem vedoucím ke snížení dávky byla trombocytopenie (nízký počet krevních destiček), která se vyskytla u 14% pacientů.
Závažné nežádoucí účinky se vyskytly celkově u 49% pacientů; nejčastěji byly hlášeny pneumonie (9%) a neutropenie (5%). Druhé primární malignity se vyskytly u pěti pacientů; z toho čtyři měli malignity s kožními projevy. Celkově 10 pacientů (6%) zemřelo na vedlejší účinky spojené s léčbou.
Dávkování
Melflufen se podává intravenózní infuzí (do žíly). V klinických studiích byla dávka:
- 40 mg melflufenu první den každého léčebného cyklu
40 mg dexamethasonu (snížená dávka pro pacienty ve věku 75 let nebo starší) 1., 8., 15. a 22. den každého 28denního cyklu
V některých studiích byla dávka snížena u těch, u kterých došlo k nežádoucí reakci.
Vedlejší efekty
Mezi nejčastěji pozorované nežádoucí účinky melflufenu patří:
• Nízký počet krvinek - neutropenie a trombocytopenie
• Anémie
• Únava
• Infekce, včetně pneumonie a infekcí horních cest dýchacích
• Nevolnost a průjem
Protože melflufen je relativně nový lék, mohou se objevit nové nežádoucí účinky, které dosud nebyly hlášeny.
Rizika
Vzhledem k tomu, že výzkum probíhá, je obtížné posoudit rizika užívání melflufenu pro RRMM. Vzhledem k tomu, že pacienti přijatí do klinických studií často vyčerpali předchozí léčbu, je pravděpodobné, že během léčby a po ní dojde k nepříznivým účinkům nebo dokonce k úmrtí.
Infekce jsou hlavní příčinou morbidity a mortality u pacientů s RRMM v důsledku oslabeného imunitního systému. Je důležité pravidelně sledovat příznaky infekce a co nejdříve hlásit jakékoli obavy svému lékaři.











-symptoms-and-treatment.jpg)




-works-for-stroke.jpg)